2017��̘Iˎ����ˎ�ﻯ�W�����������v�x(1)
����>>>2017��̘Iˎ����ˎ�ﻯ�W�����������v�x�R��
����>>>�Pע����ԇ�Ɉ̘Iˎ�����ţ��@ȡ���A�����Y��
| ��һ�� ˎ�ﻯ�W�Y���c�w�������D�����Pϵ | |
| ��һ�� ˎ��Ĺ��܈F������(��I�������D��) | �ڶ��� ˎ��ĽY�Ϸ���(�ڢ�������Y��) |
������һ�� ˎ�ﻯ�W�Y���c�w�������D�����Pϵ
������������
����1.���x����ø�������£���ˎ���D׃�ɘO�Է��ӣ����ų��w����^�̣��Q��ˎ����x
����2.�о�Ŀ�ģ��U��ˎ���������c�����Õr�̡��a���������õ�ԭ��
����3.ˎ�����w�ȴ��x�Ļ��W׃�����(���)
����ˎ����x�ķ��(�փ���)
������I�ࣺ�����D��(���܈F�ķ���)
����ˎ������M��������߀ԭ��ˮ�⡢�u�����������ʹ���ӱ�¶���O�Ի��F(�u�����Ȼ���������������)��
������II�ࣺ����Y��(�Y�Ϸ���)
����I��Įa���c�w�ȃ�Դ�Է���(������ȩ�ᡢ���ᡢ�ʰ��ᡢ������)���r�I�Y������ˮ���Ե����|���ų��w�⡣
������һ����ˎ��Ĺ��܈F������(��I�������D��)
�����ł����}����Ҫ�w�飺����(�u����)��߀ԭ��ˮ��
����һ�������h��ˎ��(����)
�������h�� ���������ɷ�����һ�������wλ��С��λ��
������������Ӣ
����һ�����h�u����
����
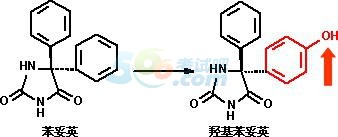
����������ϩ�I��Ȳ�I��ˎ��(����)
����������h��������D������u��������
�����������R��ƽ
�������h��������(���Գɷ�)�����Mһ���D������u��������
����
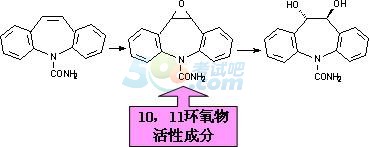
�����������̼ԭ�ӵ�ˎ��(����)
����1.�������u��
����2.�L̼朶˻��ļ��M�Ц����������Ȼ����ء�1�������u��������
����3.�ʻ���̼�����������u��������
���������������ʻ���̼���u��������
����
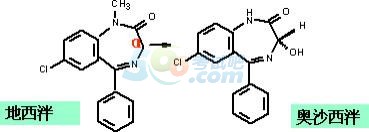
�����ġ����u�صĴ��x(����Ó�u)
����һ�����u���N�c�����ĽY���ų������������Ó�u�����ɻ������g�w���a�����ԡ�
����������ù�ض������������������ȣ��a������
�����塢���ˎ��
����N�����������N������
�������������堖
����
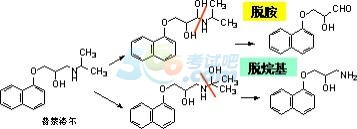
�����尷�ͺ������s�h�N����������
����
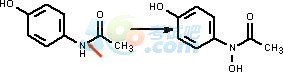
��������������ˎ��
����O��Ó���������������ͪ��߀ԭ
���������ˎ�O��Ó���
�����ɴ���
����
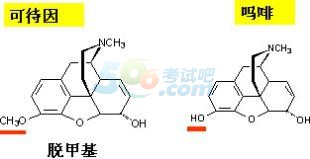
����ͪ��߀ԭ�������ɴ�
����������ɳͪ��߀ԭ����ɳ������������̼
����
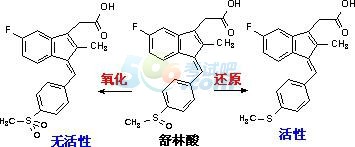
�����ߡ������ˎ��
�����c����ƣ�S��Ó���������������߀ԭ
����������������ǰ�wˎ����w��߀ԭ�������ѻ�������л��ԡ�
����
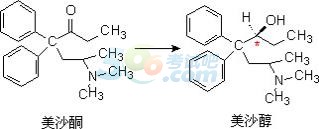
�����ˡ���������ˎ��(߀ԭ)
����1.������߀ԭ���ɷ��㰷�
����
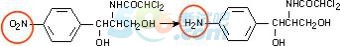
����2.���g���^�u�����g�w�����°��ͮa��������
�����š���������ˎ��Ĵ��x(ˮ��)
����1.���������Ĵ��x;����ˮ�ⷴ��
����2.�����^��ˮ���^��
����3.���������Ŀ�ˮ���Կ�����ǰˎ�OӋ





�̘Iˎ���f�}�����dح������"��ԇ�Ɉ̘Iˎ����ԇ"
| �̘Iˎ��QQȺ�� |
|---|
�������P���]��
�����f�}�죺�̘Iˎ������Ŀ���}ÿ��һ�}�R��
��2018��̘Iˎ������ˎ���I֪�R����֪�R�v��(29) (2018-05-09 14:58:29)
��2018��̘Iˎ������ˎ֪�Rһ�������俼�Pӛ(30) (2018-05-09 14:51:54)
��2018��̘Iˎ������ˎ֪�Rһ�������俼�Pӛ(29) (2018-05-09 14:42:18)
��2018��̘Iˎ��ˎ�¹����c��Ҏ�����Y��(30) (2018-05-09 14:34:24)
��2018��̘Iˎ��ˎ�¹����c��Ҏ�����Y��(29) (2018-05-09 14:30:22)
�����M���} ��ģ��ԇ�}


- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- ˎ�W����
- ˎ�W�C��
- ��ˎ��һ
- ��ˎ����
�����ęn | ���h�Y�� | ���h��Ո�� | ���h־Ը�� | �����Ԃ� | �D����Ո�� | ˼��R�� | ���˺��v | ���vģ�� | ���v���� | ����Ӌ�� | �������Y | �����u�y
�����u�y | �罻�u�y | �I�u�y | �\���u�y | ��� | ������� | �������Y | ������` | �ĵ��w�� | ����� | �{���� | �o���
�����ĕ� | ��ͬ���� | ���v���� | ����>>
Ӣ�Z�W�� | �����Z | ��x���� | ���g�Ļ� | ȤζӢ�Z | �W������ | Ӣ�Ľ������ | ÿ���n�� | ����Ӣ�Z | �ك�Ӣ�Z | ӰҕӢ�Z | Ӣ�ĸ��� | ����>>
������ȫ | ���� | С�W | ���� | ���� | Ԓ�}���� | ���� | ������ Ȥζ���� | �w������ | ӛ���� | �hՓ�� �f���� | ������ | �x��� | �����ز� | ���Ծ���
�������� | �������� | Ԋ�~�p�� | ���Z֪�R | ���� | ����ָ�� | �����c�u | �����p�� | �������A | Ԓ�}�ݾ� | ���Ľ̌W | ����>>



 ���d
���d









